Michał Antoszczak, Sebastian Müller, Tatiana Cañeque, Ludovic Colombeau, Nelson Dusetti, Patricia Santofimia-Castaño, Christine Gaillet, Alain Puisieux, Juan Lucio Iovanna, Raphaël Rodriguez: Iron-sensitive prodrugs that trigger active ferroptosis in drug-tolerant pancreatic cancer cells, Journal of the American Chemical Society 2022, 144, 26, 11536–11545. https://doi.org/10.1021/jacs.2c03973
Brak równowagi fizjologicznej i późniejszy niekontrolowany podział komórek powoduje powstanie masy tkankowej zwanej nowotworem. Zapoczątkowanie procesu nowotworzenia wymaga szeregu zmian biochemicznych, w tym zachodzących na poziomie (epi)genetycznym. Nowotwory są fenotypowo niejednorodne, co znacząco utrudnia selektywne celowanie w poszczególne komórki guza przy udziale związków małocząsteczkowych. Paradygmat dotyczący macierzystych komórek nowotworowych (ang. cancer stem cells, CSCs) opisuje subpopulację komórek o wysokiej zdolności do samoodnawiania oraz przerzutowania z miejsca pierwotnego do odległych tkanek i narządów. CSCs, zazwyczaj oporne na działanie konwencjonalnych metod leczenia, mogą powodować nawroty choroby. Poszukiwanie kandydatów zdolnych do selektywnego niszczenia CSCs jest priorytetem dla wielu zespołów badawczych i powinno przyczynić się potencjalnie do rozwoju nowoczesnych metod leczenia onkologicznego.
W trakcie badań przesiewowych przeprowadzonych w 2009 roku (Gupta et al., Cell 2009, 138, 4, 645‒659) naturalny jonofor polieterowy ‒ salinomycyna ‒ został zidentyfikowany jako najbardziej skuteczny związek wobec CSCs piersi. Salinomycyna była aktywniejsza od blisko 16 tys. innych substancji użytych w testach, w tym blisko 100-krotnie bardziej aktywna od powszechnie stosowanego w walce z tym typem nowotworu leku cytostatycznego – paklitakselu. Chemiczna modyfikacja struktury salinomycyny prowadząca do otrzymania pochodnych o wyższym potencjale przeciwnowotworowym od związku natywnego, w tym wobec CSCs, jest zadaniem aktualnym i niezwykle ważnym.
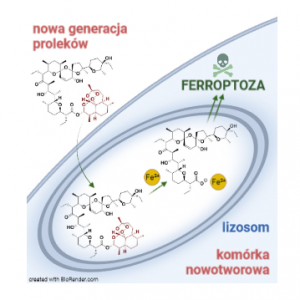
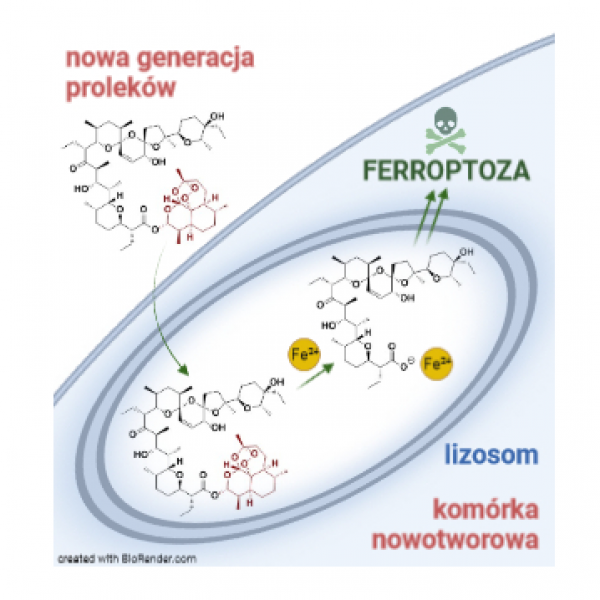
Żelazo może pełnić podwójną rolę w komórkach, zarówno stymulując ich wzrost, jak również powodując śmierć (ferroptozę). Rodzi to pytanie o możliwą funkcjonalną rolę żelaza w zwalczaniu nowotworów. Ostatnie odkrycia udowadniają występowanie homeostazy tego mikroelementu w komórkach nowotworowych, w tym tych o cechach CSCs, wskazując żelazo oraz procesy, w których ono pośredniczy, jako potencjalnie nowe cele w walce z chorobami nowotworowymi. W publikacji autorstwa dra Michała Antoszczaka z Zakładu Chemii Medycznej Wydziału Chemii UAM oraz zespołu prof. Raphaëla Rodrigueza z Instytutu Curie w Paryżu przedstawiono wyniki badań dotyczące opracowania nowego rodzaju proleków salinomycyny, w których żelazo z jednej strony działa jako chemiczny wyzwalacz poszczególnych komponentów, a z drugiej jest mechanistycznym celem dla tych związków. Eksperymenty przeprowadzone na hodowlach komórkowych 2D oraz 3D umożliwiły zidentyfikowanie struktur wiodących oraz wyjaśnienie ich przeciwnowotworowego mechanizmu działania. Proleki, będące hybrydami salinomycyny i dihydroartemizyniny, gromadząc się preferencyjnie w lizosomach, mogły reagować z żelazem, co prowadziło do uwolnienia aktywnych biologicznie cząsteczek, a następnie wywoływało ferroptozę w modelu ludzkich CSCs piersi, lekoopornych komórkach nowotworu trzustki oraz organoidach pochodzących z biopsji gruczolakoraka przewodowego trzustki. To odkrycie ukazuje znaczenie aktywnej formy ferroptozy ‒ pomijanej wcześniej cechy tej modalności śmierci komórkowej ‒ jako ekscytującego, nowego sposobu walki z CSCs i przetrwałymi, lekoopornymi komórkami nowotworowymi. Praca ta otwiera również drogę do projektowania nowych leków przeciwnowotworowych działających poprzez aktywną ferroptozę.
Publikacja jest efektem podoktorskiego stażu naukowego dra Michała Antoszczaka w zespole prof. Raphaëla Rodrigueza, który sfinansowany został przez Narodowe Centrum Nauki w konkursie Uwertura 3 (nr 2019/32/U/ST4/00092) oraz Narodową Agencję Wymiany Akademickiej w programie im. Mieczysława Bekkera, edycja 2019 (PPN/BEK/2019/1/00034).