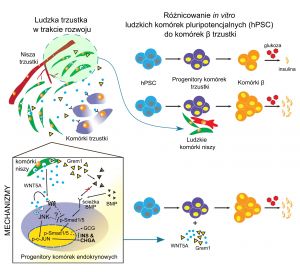
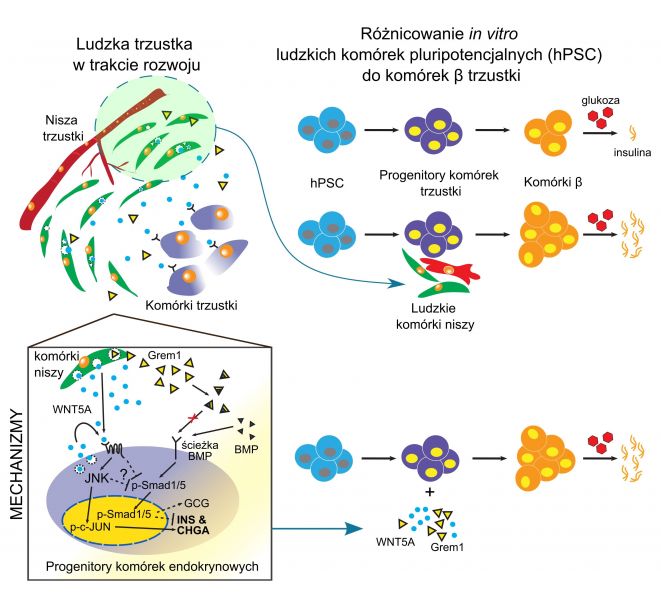
Human pancreatic microenvironment promotes β-cell differentiation via non-canonical WNT5A/JNK and BMP signaling
Jolanta Chmielowie, Wojciech J Szlachcic, Diane Yang, Marissa A Scavuzzo, Katrina Wamble, Alejandro Sarrion-Perdigones, Omaima M Sabek, Koen J T Venken, Malgorzata Borowiak
Nat Commun. 2022 Apr 12;13(1):1952.
Cukrzyca stanowi rosnący problem na całym świecie w związku z szybko rosnącą liczbą pacjentów. Cukrzyca charakteryzuje się podwyższonym poziomem glukozy we krwi, który jest spowodowany niewystarczającą ilością insuliny, hormonu umożliwiającego wnikanie glukozy do komórek obwodowych i tym samym usuwanie glukozy z krwi. Niedobór glukozy spowoduje, że niektóre komórki będą głodować i ostatecznie umrą, jak neurony, podczas gdy w innych typach komórek deficyt glukozy wywoła znaczące zmiany metaboliczne. Ponadto, nagromadzenie glukozy we krwi doprowadzi do systematycznych uszkodzeń w zasadzie wszystkich narządów w ludzkim ciele. Cukrzyca jest doskonałym celem dla medycyny regeneracyjnej, ponieważ istnieje tylko jeden rodzaj komórek, które produkują insulinę u ludzi, a są to endokrynne komórki beta trzustki. Dlatego jeśli uda nam się znaleźć nowe, wydajne źródło ludzkich komórek beta, które można przeszczepić pacjentom, możemy znaleźć nie poprawę, ale metodę wyleczenia cukrzycy.
W tym projekcie zadaliśmy proste, ale kluczowe pytanie, w jaki sposób mikrośrodowisko wpływa na rozwój komórek beta trzustki produkujących insulinę u człowieka. Najpierw ustaliliśmy, że mikrośrodowisko, zdefiniowane jako połączenie komórek mezenchymalnych i komórek śródbłonka, różni się znacząco na przestrzeni rozwoju ludzkiej trzustki oraz że tylko mikrośrodowisko specyficzne dla danego etapu jest skuteczne przy tworzeniu komórek beta z ludzkich pluripotencjalnych komórek macierzystych. Następnie zapytaliśmy, co jest takiego szczególnego, innego w tych komórkach mezenchymalnych i śródbłonkowych na tym konkretnym etapie, a stosując sekwencjonowanie RNA zidentyfikowaliśmy grupę czynników wzrostu i składników macierzy zewnątrzkomórkowej specyficznie wydzielanych na danym etapie rozwoju. W ramach równoległych wysiłków zidentyfikowaliśmy transkryptomy prekursorów komórek beta pochodzących z ludzkich komórek macierzystych i szukaliśmy par cząsteczek sygnałowych, w których ligand jest wytwarzany przez komórki mezenchymalne i komórki śródbłonka, podczas gdy prekursory komórek beta prezentują odpowiednie receptory, dzięki czemu są w stanie odpowiedzieć na te sygnały. Następnie rozpoczęliśmy najbardziej pracochłonną część projektu, w której testowaliśmy rolę każdego takiego modułu sygnałowego podczas różnicowania ludzkich komórek macierzystych w kierunku komórek beta. W rezultacie zidentyfikowaliśmy Wnt5a, czynnik wzrostu, który specyficznie wzmacniał tworzenie ludzkich komórek beta in vitro, a także poprawiał ich funkcję, czyli wydzielanie insuliny w odpowiedzi na rosnącą koncentrację glukozy. Następnie przeprowadziliśmy kolejną globalną analizę transkryptomu, aby odkryć mechanizm molekularny stojący za aktywnością Wnt5a sprzyjającą tworzeniu komórek beta. Dało nam to kilka cennych wskazówek, wyselekcjonowanych/wybranych sieci sygnalizacyjno-transkrypcyjnych, które dalej badaliśmy przy użyciu wielu reporterów lucyferazy lub obrazowej cytometrii przepływowej, co łącznie sugeruje, że Wnt5A najpierw aktywuje szlak sygnałowy c-Jun w różnicujących się komórkach beta, a następnie Wnt5a hamuje sygnalizację BMP4. Te skoordynowane sygnały wspólnie znacząco poprawiają formowanie i funkcjonowanie ludzkich komórek beta in vitro.