Magdalena Derbis, Emre Kul, Daria Niewiadomska, Michał Sekrecki, Agnieszka Piasecka, Katarzyna Taylor, Renate K. Hukema, Oliver Stork & Krzysztof Sobczak: Short antisense oligonucleotides alleviate the pleiotropic toxicity of RNA harboring expanded CGG repeats. Nat Commun 12, 1265 (2021).
1 na 5000 mężczyzn po 50. roku życia może rozwinąć neurodegeneracyjną chorobę zwaną zespołem drżenia i ataksji związaną z łamliwym chromosomem X (FXTAS, ang. fragile X-associated tremor/ataxia syndrome). Wspólnie z zespołem wrodzonego upośledzenia umysłowego i autyzmu u dzieci (FXS, ang. fragile X syndrome) oraz z zespołem przedwczesnego wygaśnięcia czynności jajników (POI, ang. primary ovarian insufficiency), patomechanizm FXTAS wynika z nieprawidłowości w budowie genu FMR1, zlokalizowanego na chromosomie X.
Jako genetyczne podłoże FXTAS wskazuje się obecność powielonej liczby powtórzeń trójnukleotydowych CGG zlokalizowanych w niekodującym fragmencie 5’ genu FMR1. U osób zdrowych najczęściej obserwuje się około 30 powtórzeń. W momencie, gdy liczba powtórzeń CGG osiągnie wartość pomiędzy 55-200, ich obecność prowadzić będzie do pojawienia się choroby. Pierwsze objawy kliniczne pojawiają się między 50. a 60. rokiem życia. Najczęściej jest to drżenie zamiarowe dłoni dominującej oraz ataksja. W dalszej fazie choroby dochodzą tzw. objawy parkinsonowskie, niestabilność chodu z upadkami, zaburzenia autonomiczne, zaburzenia funkcji poznawczych i wykonawczych, zaburzenia intelektualne i psychiczne, neuropatia w kończynach dolnych. Na dzień dzisiejszy leczenie FXTAS ma jedynie charakter objawowy.
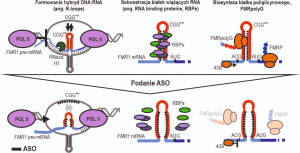
W publikacji wyników uzyskanych przez zespół profesora Krzysztofa Sobczaka z Laboratorium Terapii Genowej, będącego częścią Zakładu Ekspresji Genów na Wydziale Biologii UAM, we współpracy z zespołem profesora Oliviera Storka z Zakładu Genetyki i Neurobiologii Molekularnej z Uniwersytetu Otto von Guericke w Magdeburgu, autorzy podjęli się zbadania potencjalnego zastosowania chemicznie zmodyfikowanych cząsteczek (ASOs, ang. antisense oligonucleotide steric blockers), mających za zadanie przyłączenie się do powtórzeń trójnukleotydowych CGG zlokalizowanych w genie FMR1 i tym samym przywrócenie prawidłowego mechanizmu działania badanego genu. Uzyskane w pracy wyniki wykazały, że użycie testowanych cząsteczek w badanych liniach komórkowych, pozyskanych od pacjentów FXTAS, złagodziło molekularne objawy choroby. Dodatkowo zostały przeprowadzone testy na mysim modelu choroby. I tak, już po 3 miesiącach od podania badanych cząsteczek do płynu mózgowo-rdzeniowego myszy, wykazano niemal całkowitą poprawę w koordynacji ruchowej u chorych zwierząt. Uzyskane w pracy wyniki stanowić mogą światełko w tunelu dla osób cierpiących na FXTAS, ale również na inne genetyczne choroby, gdzie podanie ASO przywróciłoby prawidłowe działanie zmienionego genu.